|
「抗生物質」と「抗菌薬」の関係
・抗生物質(Antibiotics)とは「微生物が産生する物質のうち、他の微生物の増殖を抑える物質」のことを 指し、抗菌薬(Antibacterial drugs)とは「細菌の増殖を抑える薬品」のことを指す。 ・すなわち、抗生物質は天然物質であり、抗細菌物質だけでなく抗真菌物質なども含むことになる。 (植物が産生する抗菌物質は天然物質であるが、抗生物質とは呼ばれない。あくまで微生物が産生するもの に限られているようである。) ・一方、抗菌薬とは抗菌力のある天然物質と人工合成薬を含めた言い方であり、抗細菌薬のことを指す。 (従って、抗真菌薬や抗ウイルス薬とは区別される。) ・抗生物質はやがてその分子構造が人工的に改変され、もはや微生物が本来産生する物質とは程遠いものが 殆どである。 ・従って、現代において、細菌の増殖を抑える薬品の総称としては、「抗生物質」よりも「抗菌薬」の方が 妥当である。しかしながら、昔からの習慣でついつい「抗生物質」と呼ばれてしまうのが現状である。 たいていの生物は、他の生物種に影響を与えながら生きている
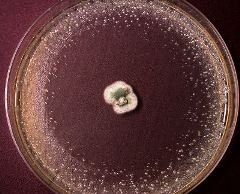
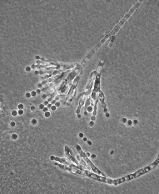
・ここで取り上げる抗生物質の話に限らず、地球上で生活する生物は多かれ少なかれ他の生物種に影響を与えながら生きている。(例えば、セイタカアワダチソウは根から cis-dehydromatricaria ester と呼ばれる毒 成分を根から分泌して他種植物の生育を抑制し、高濃度になると自らをも抑制してしまう。あるいは、ヒト に対する毒を持つ動物、植物、菌類はたいへん多い。) ・これらの毒は最初から意図されたものではなくて、自然な遺伝的変異によって生み出された成分が、偶然に も自らの生存に有利に働いたために定着したのだと解釈したい。 ・そのような毒のうち、微生物が作るものであって、ヒトにはあまり害を与えず、ヒトに感染症を起こさせる 病原菌に対してのみ害を与える(抗菌力を示す)ものが抗生物質である。 抗生物質として発見された第一号はアオカビが産生するペニシリン
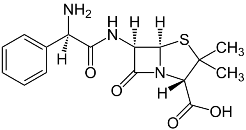
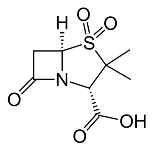
Penicillium(アオカビ属)から採れたから Penicillin
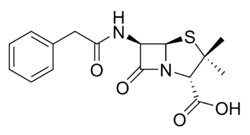
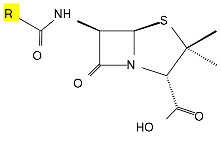
あった。 ・発見当初に「ペニシリン」と名付けられた物質は実際は混合物であって、その後に各種成分に単離精製され、 それぞれペニシリン G、N、X、F、Kなどと命名さた。
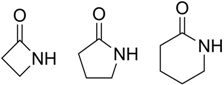
ペニシリンは細菌の細胞壁合成を阻害する
ただし、全ての真正細菌に効くわけではなかった
ペプチドグリカン合成の最終段階に関与する。 ・PBPは何種類も存在し、大腸菌では7種類とされる。(その働きから分類するならば、トランスグルコシ ラーゼ、トランスペプチダーゼ、カルボキシペプチダーゼ等である。) ・ペプチドグリカン合成酵素が1種類でも阻害されると、健全な細胞壁が形成されず、細菌の分裂に伴って、 その細胞壁は薄くなり、増殖が抑制される(静菌作用)。 ・また細菌細胞質の浸透圧は動物の体液よりも一般に高いため、細胞壁が薄くなると溶菌(破裂)を起こして 死滅する(殺菌作用)。 (=対象が菌体内に毒素を持っており菌体が破壊されると困る場合には使ってはいけない。) ・ただし、全ての真正細菌に対してペニシリンGが効くわけではなかった。例外も多くあるので一概には言え ないが、効くか効かないかのおおよその傾向は次のようである。 アオカビが日常的に競合する機会の多かった菌に対してはよく効いた ペプチドグリカン層の薄い菌には効果がなかった ・まず、生物学的・遺伝学的観点からであるが、有用な表現型をプログラムしている遺伝子は維持されるが、 使われないものの遺伝子は維持されない。すなわち無駄なものは残さないのが生物である。アオカビが生え るところには大腸菌は居ないかわりに、ブドウ球菌などのスタフィロコッカス属(Staphylococcus属)は たくさん居る。従って、ペニシリンGは大腸菌には効きにくいが、スタフィロコッカス属にはよく効いた。 (敢えて過去形にしている)。 ・次に細菌学的特徴であるが、ペニシリンGが効きにくい真正細菌は、グラム陰性の細胞壁構造を持った桿菌 (グラム陰性桿菌)である。大腸菌や緑膿菌がこれに該当する。効きにくい理由としては次のようなことが あげられる。 ① 細菌の細胞壁の構造や細胞壁外にある粘質物の有無などによって、ペニシリンGの菌体内への浸透性は大 きく違ってくる。一般的にグラム陰性桿菌ではペニシリンGが浸透しにくい。グラム陰性菌の中でも特に 強い薬剤耐性を示す緑膿菌では、菌体内と菌体外を通じるポーリンと呼ばれる小孔が小さいと言われて いる。 ② 細菌自体が薬物を菌体外へ排出する機構を持っている(大腸菌で確認済みであり、緑膿菌も同様なメカニ ズムを持っていると言われている)。 ③ グラム陽性菌の細胞壁のペプチドグリカン層は厚く、これが不完全になると溶菌しやすいが、グラム陰性 菌の細胞壁に占めるペプチドグリカン層は薄く、これがたとえ不完全になっても溶菌を起こし難い。 細菌は一方的にやられているわけではない
ペニシリンGを分解するペニシリナーゼを産生して対抗
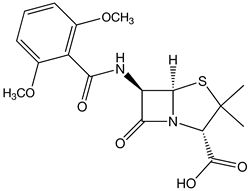
は総称してβ-ラクタマーゼと呼ばれるようになった。一般的には菌体外に分泌して、抗生物質が入ってくる 前に分解してしまう。 ・ペニシリナーゼの遺伝子がいつ生まれたのかは定かではないが、アオカビがペニシリンを分泌してきたから には、それに触れてきた微生物は抵抗する手段としてペニシリナーゼの遺伝子を獲得していたに違いない。 ただ、人間によるペニシリンGの大量使用によってペニシリナーゼ遺伝子も様々な細菌に急速に広まったこと は間違いない。(細菌同士はプラスミド (plasmid) の授受やバクテリオファージなどのベクターを通じて容 易に遺伝子交換する。) ペニシリナーゼで分解されない半合成抗生物質、「メチシリン」登場
人間が新たな病原微生物であるMRSAを生み出してしまった
ペニシリン系抗生物質の種類が増えればそれに伴って
細菌が作るβ-ラクタマーゼの種類もどんどん増えてきた
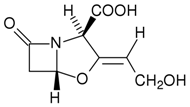
(別ページにて紹介する)が、細菌は、そのそれぞれに対抗できるβ-ラクタマーゼを生み出してきた。 ・β-ラクタマーゼの種類は現在のところ、そのアミノ酸配列や、関与する細菌遺伝子の塩基配列の相同性を 元に、A~Dの4クラスに分類されており、上述のペニシリナーゼはAクラスに属する。しかし、その分類に 当てはまらないものも登場してきている。(例 : Extended Spectrum β-Lactamases。略してESBLs。 より多くのβ-ラクタム系抗菌薬を分解できるβ-ラクタマーゼ。) 人間は、細菌が作るβ-ラクタマーゼを阻害する薬物も併用してきた β-ラクタマーゼ阻害薬もβ-ラクタム環を持つ
・今後もβ-ラクタム系抗生物質を使い続ける限り、細菌の遺伝的変異や異種細菌同士の遺伝子交換によって、 β-ラクタマーゼの種類や、その遺伝子を持つ耐性菌は増え続けるであろう。これはどの系統の抗菌薬につい ても同じことが言える。 ・耐性菌の出現を最小限にくい止めるためには、あらゆる抗菌薬をより慎重に使用することである。標的に する病原菌の種類と薬剤耐性などの特徴を確実に見極め、無駄な薬剤使用にならないよう努めることである。 ・これまで、抗菌スペクトラムの広い抗生物質の開発が行われてきたが、理想的には標的とする菌種のみに 効いて、その他の菌には影響を与えない薬物が理想である。ペニシリンなどの抗菌スペクトラムの狭い薬剤 は古くてもそれなりに貴重なものである。 <関連リンク> ◆セフェム系 ◆サルファ薬・ST合剤 ◆ニューキノロン系 ◆細菌感染症 ◆寄生虫疾患・原虫疾患 ◆真菌症 ◆マイコプラズマ・リケッチア・クラミジア感染症 ◆ウイルス感染症 |
|||||||||||||||||||||