◆ はじめに
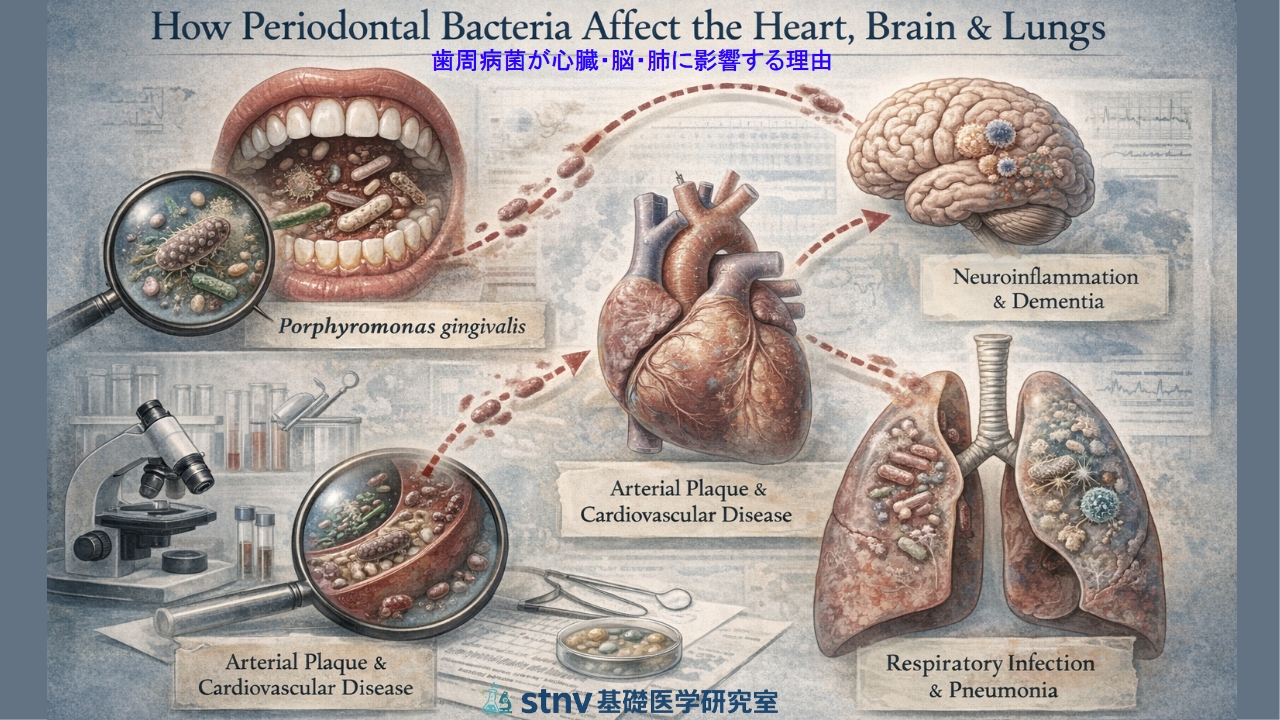
歯周病は「口の中だけの病気」と思われがちですが、近年の研究はまったく異なる姿を示しています。歯周病菌は、口腔という局所にとどまらず、血流や気道を通じて全身へと広がり、心臓・脳・肺といった重要な臓器に“静かな炎症”をもたらすことが分かっています。特に、Porphyromonas gingivalis(P. gingivalis)をはじめとする歯周病関連細菌は、血管内皮の炎症、動脈硬化の進行、脳内の神経炎症、さらには誤嚥性肺炎やCOPDの悪化にまで関与している可能性が指摘されています。
口腔は、全身の炎症反応を左右する“起点”となる場所です。今回の記事では、歯周病菌がどのようにして心臓・脳・肺へ影響を及ぼすのか、そのメカニズムを生態系の視点から見ていくことにします。
◆ 口腔は“微生物の密集地帯”である
口腔には、平均的に見るならば、小腸の中〜下部に匹敵する量の微生物(細菌・真菌・ウイルスなど)が存在していると捉えて結構です。もちろん、個人差も大きく、口腔の状態によっても大きく変わります。健全な口腔では微生物の多様性が高く、唾液1mLあたり10⁸〜10⁹個ほどの細菌がバランスよく共存しています。一方、軽度の歯周病になると、嫌気性菌が増え始め、総数もやや増加します。更に、重度の歯周病では微生物の多様性が大きく低下し、特定の病原性菌が優勢となり、細菌の密度も大幅に増える傾向があります。
一般的に、歯の表面にはバイオフィルム(プラーク)が形成され、歯周ポケットには酸素の少ない環境が広がり、舌の表面には複雑な凹凸が存在します。これらはすべて、微生物が棲みつきやすい“微小な生態系”です。更に、口腔は食事・会話・呼吸を通じて外界と常に接しており、微生物が出入りしやすい構造を持っています。そのため、口腔マイクロバイオーム(=その場所にすむ微生物の集まり)は、外界の微生物と免疫が絶えず対話しながら成り立つ、非常に動的な生態系だということになります。
◆ 歯周病菌とは何か ──P. gingivalis を中心に
歯周病の中心的な細菌である P. gingivalis は、単なる“口の中の細菌”ではありません。この細菌は、バイオフィルムの深部で増殖し、免疫から逃れるための巧妙な仕組みを備えています。P. gingivalis のLPS(リポ多糖)は、通常の細菌の一般的なLPSとは異なり、免疫を強く刺激しない“静かな炎症”を引き起こします。また、gingipain と呼ばれる酵素を分泌し、免疫細胞の働きを乱すことによって慢性的な炎症を維持し続けます。この“静かな炎症”こそが、口腔だけでなく全身の臓器に影響を及ぼす出発点となります。
◆ 代表的な歯周病菌の P. gingivalis は、どこから来た細菌なのか
歯周病の中心的な細菌である P. gingivalis は、自然界のどこにでも存在する細菌ではありません。酸素があると生きられず、ヘム(血液成分)を必須とし、タンパク質分解産物を栄養源とするなど、きわめて特殊な条件を必要とします。このような性質は、ヒトの歯周ポケットに強く適応した結果と考えられています。では、この細菌はいつ、どのようにしてヒトに定着したのでしょうか。霊長類の進化の流れをたどると、いくつかの手がかりが見えてきます。
① P. gingivalis は「ヒトの歯周ポケット」に特化した細菌である
歯周ポケットは、酸素が少なく、炎症によって血液成分が滲み出やすいという、P. gingivalis にとって理想的な環境です。この細菌はバイオフィルムの深部で増殖し、gingipain (ジンジペイン)などの酵素を用いて免疫から逃れる仕組みを備えています。このような特徴は、ヒトの口腔という生態系に合わせて進化した“宿主依存型”の性質を示しています。
② 霊長類が誕生した頃には存在したのか?
興味深いことに、チンパンジーやゴリラなど、ヒトに近い霊長類の口腔からは P. gingivalis そのものはほとんど検出されません。近縁の Porphyromonas属は存在しますが、ヒトの P. gingivalis とは別種です。このことは、P. gingivalis が霊長類一般に広く存在していた細菌ではなく、ヒト系統の進化に合わせて特化した細菌であることを示唆しています。
③ 人類史のどの段階で出現したのか?
現在のところ、ネアンデルタール人の歯石から P. gingivalis のDNAが検出されていることが分かっています。即ち、ホモ属(Homo)の段階ではすでに存在していた可能性が高いということです。
一方で、より古い霊長類の化石からは確認されていません。このことから、P. gingivalis は、霊長類の初期には存在せず、ヒト属の進化とともに成立し、現生人類の口腔で安定した生態系を築いたと考えられています。
④ 主な感染ルートは?
上述しましたように、P. gingivalis は、自然環境に広く存在する細菌ではなく、主にヒトの口腔内で維持される細菌です。そのため、外界から偶然に取り込まれるというよりも、人から人へ、生活の中でゆっくりと受け渡されていくという特徴があります。
最も一般的なルートは、家族内での口腔接触です。親子間のスキンシップ、食器の共有、口移しなど、日常的な接触を通じて細菌が移動します。また、パートナー間の接触(キスなど)でも伝播することが知られています。このような行動は特別なものではなく、日常の中で自然に起こるため、P. gingivalis は家族単位で“共有される”傾向があります。
ただし、P. gingivalis が口腔に入ったとしても、すぐに定着するわけではありません。歯周ポケットが深くなり、酸素が少なく、炎症によって血液成分が滲み出るような環境が整って初めて、この細菌が増殖しやすい“住処”が成立します。つまり、伝播と定着は別の問題であり、定着には宿主側の環境が大きく影響します。
このように、P. gingivalis は外界から突然侵入する細菌ではなく、人と人との生活の中で受け継がれ、口腔環境が整ったときに定着するタイプの細菌です。この性質が、歯周病が家族内で似た傾向を示す理由のひとつと考えられています。
◆ 歯周病菌が全身へ広がるルートと関連疾患
歯周病が進行すると、歯ぐきの血管が露出し、細菌が血流に入り込みやすくなります。これが“菌血症”です。歯磨きや食事のたびに微量の細菌が血流へ流れ込み、全身を巡ります。また、高齢者では誤嚥によって口腔細菌が肺へ到達し、誤嚥性肺炎の原因となります。更に、歯周病によって生じた慢性炎症は、免疫系を介して全身の炎症レベルを高め、心臓・脳・肺の疾患リスクを押し上げます。
では、それぞれについて補足しておくことにします。
◇ 心臓への影響──動脈硬化と心血管疾患
血流に乗った歯周病菌は、全身の血管を巡り、その過程で血管内皮に炎症を引き起こします。特に、動脈硬化プラーク(アテローム)から歯周病菌が検出されるという報告は多く、P. gingivalis のDNAやLPSが血管壁に存在することが確認されています。
これらは血管内皮の炎症を促し、マクロファージの取り込みを増やし、結果として動脈硬化の進行を加速させます。そして、慢性的な炎症は、心筋梗塞や脳梗塞のリスクを高める要因となるわけです。
◇ 脳への影響──神経炎症と認知症との関連
近年、歯周病菌と認知症(特にアルツハイマー病)との関連が注目されています。脳内から P. gingivalis が産生する酵素(gingipain) が検出されたという報告は、医学界に大きな衝撃を与えました。gingipain は神経細胞に対して毒性を持ち、炎症性サイトカインの産生を促すことで、脳内の慢性炎症(neuroinflammation)を引き起こします。これは、アルツハイマー病の進行に関わる重要な要素の一つであると考えられます。
もちろん、歯周病菌が認知症の“唯一の原因”というわけではありません。しかし、脳の炎症を静かに高める要因として無視できないというのが、現在の科学的な位置づけです。
口腔という局所の炎症が、血流を介して脳にまで影響を及ぼす──これは、人体を“つながった生態系”として捉える視点の重要性を示しています。
◇ 肺への影響──誤嚥性肺炎とCOPD悪化
高齢者に多い 誤嚥性肺炎 の主因は、実は口腔内の細菌です。食事中や睡眠中に微量の唾液が気道へ流れ込むことは珍しくありませんが、口腔内の細菌が多い場合、そのまま肺へ到達し、炎症を引き起こします。特に、歯周病菌や舌苔に多い嫌気性菌は、肺に到達すると強い炎症反応を誘発し、誤嚥性肺炎の原因となります。これは、口腔ケアが肺炎予防に有効である理由のひとつです。
また、COPD(慢性閉塞性肺疾患)の急性増悪にも口腔細菌が関与している可能性が指摘されています。口腔内の細菌が気道に流入し、炎症を悪化させることによって、呼吸機能をさらに低下させてしまうのです。
要するに、口腔は肺と直接つながっており、口腔マイクロバイオームの状態が呼吸器の健康を左右するということになります。
◆ まとめ──口腔は全身の“炎症ネットワーク”の起点である
歯周病菌は、口腔という局所にとどまらず、血流や気道を通じて心臓・脳・肺へと影響を及ぼします。その背景には、微生物と免疫がつくる“静かな炎症”があり、これが全身の臓器に負荷をかけ続けます。
そのため、口腔マイクロバイオームを整えることは、単なる口腔ケアではなく、全身の炎症を抑え、健康を守るための基盤であると言えるわけです。
次回の記事では、P. gingivalis が“住みつけない口腔環境”をどのようにつくるのか、その実践的な方法を取り上げる予定です。